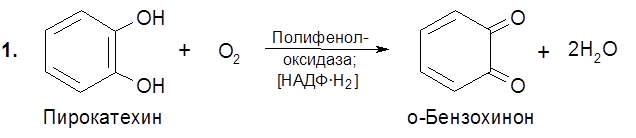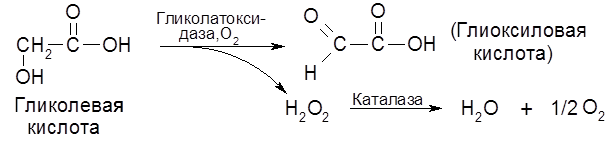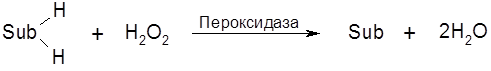| МЕТОДИЧЕСКИЕ УКАЗАНИЯ по изучению биологической химии и задания для самостоятельной работы |
 |
 |
| Добавил(а) Administrator |
| 16.02.11 13:09 |
|
Страница 8 из 19
Процессы окисления, связанные с дегидрированием, реализуются в условиях анаэробного окисления глюкозы (гликолиз, брожение), при окислительной деструкции пировиноградной кислоты и ацетил-S-КоА ( В процессе аэробного окисления в качестве акцептора (окислителя) молекул водорода на заключительных стадиях функционирует кислород. Существует три способа окислительного действия кислорода: 1. Окисление водорода до воды в дыхательной цепи. 2. Окисление водорода НАД·Н2 и НАДФ·Н2 с участием промежуточных агентов – аэробных дегидрогеназ флавинового типа. Флавопротеин – желтый дыхательный фермент, отщепляющий Н2 от НАДФ·Н2 при окислении гексозомонофосфата в фосфоглюконовую кислоту передает водород коферменту ФАД·Н2 и далее – кислороду воздуха. 3. Третий путь окисления связан с непосредственным воздействием окислителя на субстрат с внедрением в его структуру одного или двух атомов кислорода (А.Н. Бах). Окисление такого типа осуществляется так называемыми “прямыми” оксидазами и не сопровождается образованием АТФ. 4.4. Цитохромы и их предшественники.
Ферменты цитохромы, обозначаемые латинскими буквами (а, а3, в, в3, в6, в7, с, с1, d, f, o и др.), представляют собой протеиды (белки), содержащие в качестве простетических групп гемы. Последние являются порфириновыми комплексами железа. Физиологическая функция цитохромных систем заключается в окислении кислородом молекул водорода, в частности, в цикле трикарбоновых кислот. Цитохромы существуют в окисленной и восстановленной формах, легко превращающихся друг в друга в результате переноса электрона:
В качестве промежуточных звеньев в переносе электронов молекул водорода от восстановленных анаэробных дегидрогеназ к кислороду выступают наряду с цитохромами флавопротеиды (флавинзависимые дегидрогеназы), негемовые железопротеиды (ферредоксины) и жирорастворимые хиноны (убихиноны, или коферменты Q). Процессы аэробного окисления у клеток прокариот локализованы в клеточной мембране, а у эукариот – в митохондриях. Ферментативное окисление молекулярным кислородом катализируется оксигеназами. Некоторые из них выступают в качестве аэробных дегидрогеназ – отщепляя от субстрата водород, они превращают его в воду или пероксид водорода. Другие обеспечивают внедрение в молекулу субстрата двух атомов кислорода, сопряженное в ряде случаев с расщеплением ароматических или алициклических колец. Оксигеназы третьего типа, называемые гидроксилазами, внедряют в субстрат один из двух атомов молекулы кислорода. Типичными представителями оксигеназ являются полифенолоксидазы (фенолоксигеназы).
В растениях широко распространен фермент липооксидаза (липооксигеназа), обусловливающий окисление кислородом воздуха некоторых ненасыщенных длинноцепных жирных кислот и образуемых ими сложных эфиров, в частности, жиров. Липоксигеназа разрушает каротин в процессе сушки и хранения растительных продуктов, а также обусловливает прогоркание масел, круп и муки. К группе “прямых” оксигеназ относится уратоксидаза (уриказа). В растениях содержится оксидаза гликолевой кислоты – гликолатоксидаза:
В плесневых грибах содержится фермент глюкозооксидаза, способная окислять глюкозу в глюконовую кислоту. Ферментами прямого биологического окисления являются каталаза и пероксидаза. Биологическая функция каталазы заключается в разложении пероксида водорода:
Пероксидаза катализирует окисление субстратов (
Пероксидаза содержится в слюне, соке поджелудочной железы, печени, лейкоцитах, в корне хрена, в млечном соке растений. Выделена и охарактеризована пероксидаза хрена (гемопротеид, М=40,000).
5.1. Наиболее важные представители – строение и свойства. 5.2. Обмен углеводов – анаболизм и катаболизм. Брожение и аэробное окисление. 5.2.1. Гликолиз. 5.2.2. Пировиноградная кислота. 5.2.3. Цикл трикарбоновых кислот (ЦТК, цикл Кребса). 5.2.4. Глиоксилатный цикл. 5.2.5. Пентозофосфатное (апотомическое) окисление моносахаридов. 5.2.6. Особенности обмена углеводов в организмах животных и человека. 5.2.7. Аэробный распад (брожение) углеводов (сахаров). 5.2.8. Фотосинтез. 5.2.9. Взаимопревращения углеводов в растительных организмах. 5.2.10. Хемосинтез. 5.1. Наиболее важные представители – |
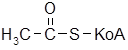 ) в цикле трикарбоновых кислот (ЦТК), в пентозофосфатном окислении глюкозы, в реакциях
) в цикле трикарбоновых кислот (ЦТК), в пентозофосфатном окислении глюкозы, в реакциях