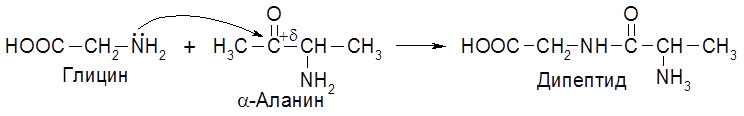| МЕТОДИЧЕСКИЕ УКАЗАНИЯ по изучению биологической химии и задания для самостоятельной работы |
 |
 |
| Добавил(а) Administrator | ||||||||||||||||||||||||||||||||||||||||||
| 16.02.11 13:09 | ||||||||||||||||||||||||||||||||||||||||||
|
Страница 15 из 19
Кофермент А под влиянием трансфераз замещается ацилпереносящим белком (АПБ).
На следующей стадии образовавшийся бутирил-S-АПБ ацилирует новую молекулу малонил-S-АПБ. Далее снова реализуется декарбоксилирование Суммарное уравнение синтеза, например, пальмитиновой кислоты отражает участие семи молекул малонил-КоА.
Диссимиляция (катаболизм) жиров в растительных тканях наиболее интенсивно протекает в прорастающих семенах масличных культур. Первоначальная стадия – гидролиз глицеролов – протекает под действием фермента липазы:
Известно три типа окисления жирных кислот:
Образовавшийся ацилкофермент А подвергается окислительной деструкции по той же схеме. 6.7. Вопросы для самоконтроля 27. Дайте определение липидов и проведите их классификацию. 28. Почему жиры при хранении прогоркают? В чем суть автоокисления жиров? 29. В чем суть биологического окисления жирных кислот. Энергетическая функция кислот. Охарактеризуйте 30. Представьте механизм синтеза жирных кислот на основе малонил-КоА. 7. Белки и аминокислоты – строение,
7.1. Общая характеристика. Биологическая роль 7.2. Аминокислоты – строение и свойства 7.3. Структура и классификация белков 7.4. Биосинтез и обмен аминокислот в растительных организмах 7.5. Особенности метаболизма белков и аминокислот в животных организмах 7.6. Биосинтез белка. Нуклеиновые кислоты 7.7. Пути видоизменения ДНК: мутации, лизогения, трансиндукция, трансформация. Рекомбинация ДНК 7.1. Общая характеристика. Биологическая роль Аминокислоты и продукты их конденсации – полипептиды и белки – являются “краеугольным камнем” “здания” живой природы. В организмах животных белки составляют 14-23% свежей ткани и 45-80% сухой массы. Они являются структурными элементами мышц и тканей, внутренних органов и крови, волос и перьев, входят в состав ферментов, гормонов, антител и большого множества физиологически активных веществ. Источником белка для человека и животных являются пищевые продукты растительного и животного происхождения. Некоторые из них представлены в таблице 7.1. Таблица 7.1 Содержание белка в пищевых продуктах (%)
7.2. Аминокислоты – строение и свойства Основу белков составляют 20 аминокислот. Некоторые из них содержат кроме карбокси- и аминогрупп, другие функциональные группы (–OH, –SH, =NH и др.), ароматические ядра, азотсодержащие гетероциклы. Примеры:
Все природные аминокислоты, кроме аминоуксусной, содержат асимметрический атом углерода и относятся к L-ряду. Аминокислоты обладают всеми свойствами амино- и карбоксильных групп, в частности, их можно алкилировать и ацилировать. Важнейшим свойством аминокислот является ацилирование аминогруппы одной молекулы за счет карбоксильной группы второй молекулы.
Именно такого типа реакции лежат в основе поликонденсации ряда аминокислот в определенной последовательности, ведущей к образованию полипептидов и белков.
|
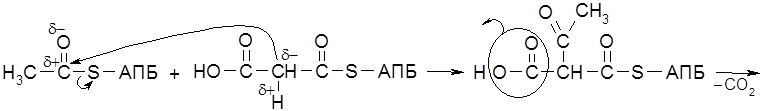

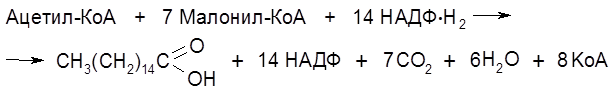
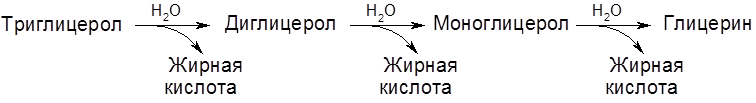
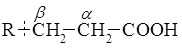 и последовательно отщепляют от нее двухуглеродные фрагменты в виде молекул ацетил-S-KoA (
и последовательно отщепляют от нее двухуглеродные фрагменты в виде молекул ацетил-S-KoA ( 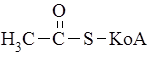 ).
).